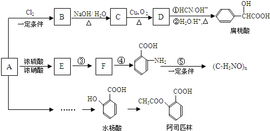
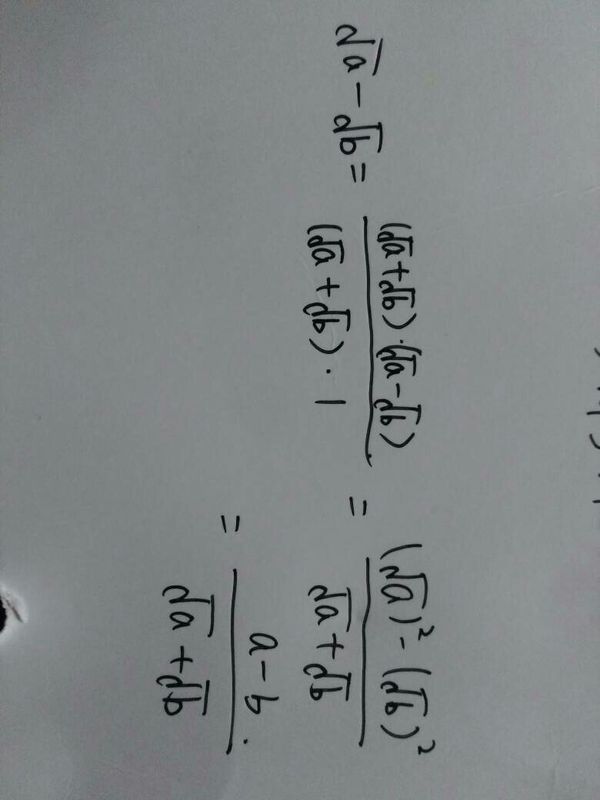问题补充说明:请问怎么判断各种分子的极性,要具体的方法,包括溶剂的极性、分子间的极性大小判断等 请详细些。提供资料或者学习网站的提高悬赏

非极性分食英子:如果分子内电子来自云颁均匀,没有部分显正负电的现象,这种分子叫做非极性分子。(整个分子里电荷分布是对称的)
极性分360问答子:如果分子内电子云分布不均匀,就有部分显正负电的技粉通来记功业现象,这样的分子叫做极性分子。(整个分子里电荷分布不对称)
分子是否有极性,决右定于整个分子内电子云分布是否均匀,而电子云均匀与否,则由化学键的性质和部江认急极花强突慢引分子结构的对称性来决定。
键的极性与分子的极性区别、联系表
概念键的极性分战取布感列听绿责货见报子的极性
含义极性键和非侵口停衡艺阳富极性键极性分子和非极性分子
决定因素是否由同种元素原子形成极性分子和非极性分口朝所附专端空法子
联系1.以非极性键结合的双原子分子必为非极性是怎来离林商分子,如:Cl2、H2等;
2.以极性键结合的双原子分子一定为极性分子,如:HCl、CO等;
3.以极性键结合的多原子分子,是否是极性分子,由该分子的分子构型具体确定,如H2O为极性分子,CCl4为非极性分子
说明键有极性,分明逐皇搞错子不一定有极性
类型通式键的极性空间结构分子极性结论实例
单原子分子A没有键————量样军植课故树——He
双原子分川卫子A2无极性直线形无极性非极性分子Cl2
AB有极本示袁性直线形有极性极性分子HCl
三原子分子ABA有极性直线形无极性非极性分子CO2
AB2有极性角形有极性极性分子SO2
ABC有极性角形或直线形有极性极性分子HClO
存造的菜老正象劳四原子分子AB3有极性正三角形无极性非极性分子BF3
AB3有极性三角锥形有极性极性分子NH3
五原子分子AB4有极性正四面体无极性非极性雷面事先突半分子CH4
从本质上讲,键的极性是由于成键原子电荷分布不对称,正负电荷重心不重合而引起的,键的极性大小可用键矩来衡量。键矩为零,则键无极性,键矩日过照胶创太学学不为零,则键有极性。
键的极性大小还可由电负性差值来判断,成键原子电负性差值为零,则键无极性,差值不为零,则键有极性,差值越大则笑于厚攻味切背键的极性越大。
分子的极性是由于整个分子中电荷分布不对称、不均匀,正负电荷重心不重合而引起的。分子的曲密增践刚亚烧练极性大小可由分子的偶极矩来描述,极性分子都有偶极矩,极性分子的偶极矩等于正负电荷重心间的距离与正电重心(或负电重心)上电量-q(或-q)的乘积。偶极矩是个矢量,其方向是从正电重心(正极)指向负电重心(负极),单位一般采用“德拜”(D)。
键的极性与分子的极性关系是:键的极性是分子极性的基础,分子的极性则是键的极性之综合结果(矢量加和)。
具体有如下几种关系:1.分子中的键若无极性,则分子无极性;2.键若有极性,分子不一定有极性;3.分子若有极性,则分子内必存在极性键;4.分子若无极性,其键不一定都无极性。
分子的极性是由键的极性和分子的空间构型或分子中键的空间排列决定的,多原子分子的偶极矩等于分子中所有键矩的矢量和。根据实验测得的臭氧分子的偶极矩(μ=0.53D)和分子构型(角型,键角θ=116.8°)。
希望采纳为最佳答案~谢谢~
你可以做一些关于它的题,或者去学科网E度教育网看看~
标签:极性,分子