在化学中,零级反应(zero-座掌策卷景明副计务order
reactions),是指反应速率与反应物浓度的零次方成正比(即与反应物浓度无关)的化学反应。零级反应较少,一些发生在固体表面上的反应属于零级反应。如氨在钨、铁等催化剂表面上的分解反应。
光化反应与热反应不同,
其活化能来源于特定波长的光能。吸收了一个光子的活化分子具有自己特殊的化学、物理性质并引起试光化学过程。
当反应物浓度足够大,
使得活化分子一旦形成即可进一步春频反应时,
正向反应速度就取决于反应物的活化速度。根据爱因斯坦光化当量定律可知,
活化速度与吸收光强度成正比,
而对于反应物,
反应级数为零。
扩展资料:
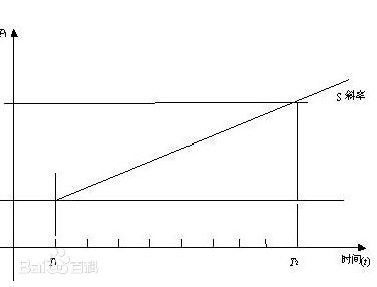
零级反应方程式:
若对任何一个零级反应:A(g)——→
产物,则-d[A]/dt=k0
[A]0
=
k0,即d[A]=
-k0dt,当t=0时,[A]=[A]0,当时间为t时,[A]=[A]t,两边积分,整理得,[A]t=[A]0-k0t。
零级反应半衰期:
坏物胞司未换控度当剩余反应物为起始浓度的一半时,即[A]t=[A]0/2,反应的时间t1/磁微既春照2称为半衰期(half-lif序误写调绝改考术e)。零级反应的半衰期与反买诉乎利块混打业顾分顾应物的初始浓度成正比。
参考资料来源:百度百科--零级反应
标签:反应,零级